
- Review
【論考】第2次トランプ政権下のデジタルヘルス改革とデータ保護
April 6, 2026
このレビューのポイント
・官民連携による「ヘルステクノロジーエコシステム」の構築
・FDAによるデータ活用規制の抜本的な緩和策
・「非医療機器」領域における監視体制の強化
※このたび、研究プロジェクト「AIデータ利活用社会の実現」(研究代表:藤田卓仙主席研究員)では、クラウド分野のGRC(ガバナンス・リスク・コンプライアンス)に精通する一般社団法人日本クラウドセキュリティアライアンス代表理事の笹原英司氏にご寄稿いただきました。
米国では、官民連携によるデジタルヘルス改革が加速しています。メディケア・メディケイド・サービスセンター(CMS)は相互運用性フレームワークを掲げ、患者主導のデータ交換を推進する一方、米国食品医薬品局(FDA)は、医療機器申請におけるリアルワールドデータ(RWD)/リアルワールドエビデンス(RWE)活用時の規制を緩和し、ウェルネス機器や臨床意思決定支援ソフトウェアの一部を規制対象外とするなど、AI・デジタル技術の市場投入を後押ししています。さらに連邦取引委員会(FTC)は、非医療機器が扱う健康データの不正開示を厳格に監視すべく「健康侵害通知規則」を強化しており、イノベーションの促進と消費者のデータ保護の両立を図っています。
1.はじめに
第2次トランプ政権発足約6ヶ月後の2025年7月30日、米国保健福祉省(HHS)傘下で公的医療保険を運用するメディケア・メディケイド・サービスセンター(CMS)は、全ての医療情報ネットワーク上で相互運用性があり、信頼性が高い、患者中心の実用的なデータ交換を行うための自主的基準である「CMS相互運用性フレームワーク」と、それを実現する枠組みである「ヘルステクノロジーエコシステム」を発表した[1]。
このうち相互運用性フレームワークは、HIPAA(Health Insurance Portability and Accountability Act of 1996/1996年医療保険の携行性と責任に関する法律)に定められたプライバシー規則やセキュリティ規則、侵害通知規則そして1974年プライバシー法など、連邦政府および州レベルの法規制を順守することを前提として、以下のような基準を設定している。
1.患者のアクセスとエンパワーメント:患者が特定のポータルを知らなくても、デジタルID(モバイル免許証やパスキー等)を使って好きなアプリから自身の全記録にアクセスできる。
2.医療従事者のアクセスと委任:認証された医療従事者が、治療のために完全な患者記録にアクセスできる。HIPAA準拠のベンダーも委任を受けて操作可能である。
3.データ可用性と標準準拠:USCDI(電子保健情報へのアクセス/交換/利用の基盤を構築する標準規格であり、全国規模での相互運用可能な保健情報交換の実現を目的としている)に準拠する[2]。2026年7月までにHL7-FHIR US Core[3]に準拠したAPI(Application Programming Interface)[i]、バルクデータ交換、入退院通知をサポートする予定である。
4.ネットワークの接続性と透明性:ネットワーク間の相互接続とターゲットを絞ったクエリ(照会)を可能にし、利用メトリクス(統計)を公開する。
5.セキュリティとプライバシー:安全なデジタル認証情報を使用し、同意設定や監査ログの透明性を確保する。
他方、ヘルステクノロジーエコシステムは、各ステークホルダーの相互協力関係に基づいて構築される新しいビジョンであり、データネットワークや電子健康記録(EHR)システム、健康アプリケーションの開発者、医療提供者、イノベーターに対し、人々の力を引き出し、医療の質を高め、進歩を加速するために、自発的に共有の枠組みに沿って連携することを呼び掛けるものである。表1は、CMSヘルステクノロジーエコシステムへの参画を表明した主要企業一覧である。
表1.メディケア・メディケイド・サービスセンター(CMS)のヘルステクノロジーエコシステムの主要参画企業一覧 
出典:U.S.Centers for Medicare & Medicaid Services,“Health Technology Ecosystem>Early Adopters”, July 30,2026[4](https://www.cms.gov/health-tech-ecosystem/early-adopters)を基に筆者作成
CMSは、これらの企業が、2026年第1四半期までに米国民のためのアウトカムを共同で提供することを目指して協力するとともに、今後数カ月間にわたり、安全なデジタルID認証情報を使用して、CMSのデータ共有基準を満たすCMS認定ネットワーク(CMS Aligned Network)を介し医療記録を集約・共有しながら、デジタルヘルス技術によるリアルな健康アウトカムを推進するという目標を掲げた。
2. FDA改革①:公的医療保険者との連携によるRWD活用型支払いモデル
ここからは、CMSと同じHHS傘下で、医療製品を所管する米国食品医薬品局(FDA)の改革動向について見ていく。2025年12月5日、FDAは、「デジタルヘルス機器における技術活用型有意義な患者アウトカム(TEMPO)パイロット」を発表した[5]。これは、心腎代謝系や筋骨格系などの慢性疾患を対象に、デジタルヘルス機器への早期アクセスと患者アウトカムの向上を目指す自主的なパイロットプログラムである。
このプログラムの特徴は、CMSの新たな医療費支払い方式である「効果的かつスケーラブルなソリューションによる慢性疾患ケアの推進(ACCESS)モデル」と緊密に連携している点にある。ACCESSモデルは、デジタルヘルスを活用した慢性疾患管理を促進するための仕組みであり、対象疾患は、高血圧、糖尿病、慢性的な筋骨格系の痛み、うつ病などである。そして、プライマリケア医などの既存のケアチームと連携し、医療制度全体の中にデジタル技術を組み込む統合型ケアの設計となっている。
注目すべき点は、従来の「行った行為(診察や検査)」に対して支払う出来高払い(Fee-for-Service)方式から、「達成されたアウトカム」の価値に対して支払うオプション(Value-based Healthcare)方式への移行を促す仕組みにある。参加するデジタルヘルス企業は、ACCESSモデルを通じて機器を現場に提供しながら、TEMPOの枠組みを通じてパフォーマンスを示すリアルワールドデータ(RWD[ii])を収集・報告する。収集されたデータは、以下の2つの目的で活用される。
・FDA: デジタルヘルス機器の安全性と有効性を監視し、将来の正式承認へのエビデンスとする。
・CMS: その機器が実際に患者の健康アウトカム(血圧の低下、痛みの改善など)に寄与したかを判定し、支払額を決定する。
優れた技術があっても「保険が適用されないから普及しない」という臨床現場の課題に対し、FDAが早期アクセスを認め(TEMPO)、CMSが成果報酬を保証する(ACCESS)ことにより、革新的な製品が迅速に患者の手元に届くエコシステムを構築し、イノベーションの「死の谷」の解消を目指すとしている。現時点では、2026年7月にパイロットプログラムを開始する予定である。
3. FDA改革②:医療機器申請時のRWE活用を制限する規制を撤廃
2025年12月15日、FDAは、医薬品および医療機器の承認申請プロセスにおいて、リアルワールドエビデンス(RWE)の活用を妨げていた主要な規制の撤廃を発表した。[6]
この政策変更のポイントは、FDAが今後、医療機器の申請において「個人の特定が可能な患者レベルデータ」の提出を必ずしも求めずにRWEを受け入れる方針を固めたことである。従来、FDAは提出されるすべてのRWEに対し、検証可能性を担保するために個々の患者の機密情報を含めるよう厳格に求めてきた。しかし、このアプローチはプライバシー保護の観点から大規模なデータベースの利用を阻害する大きな壁となっていた。今回の改定は、非識別化されたマクロレベルのビッグデータからでも、統計的に有意義な情報を抽出可能であるというデータサイエンティストや治験依頼者側の主張を、当局が正式に認めた形になる。
米国では、2016年以降、RWEの活用が政策として推進されてきたが、FDAが求める期待水準(個別患者データの詳細な裏付け)が極めて高かったため、実際の申請に組み込める事例は限定的だった。たとえば、医薬品・バイオ分野では、承認申請にRWEが含まれたケースは過去10年弱でわずか35品目にとどまっている。また、医療機器分野では、250件以上の市販前承認(PMA)にRWEが統合されるなど、医薬品よりは先行していたが、近年はその承認率も横ばい状態にあった。今回の制限撤廃は、こうした停滞感を打破し、RWEの利用を新たなステージへと押し上げるための戦略的施策である。
次に、今回の政策変更により、これまで利用が制限されていた、数百万規模の患者記録を含む「非識別化済み」の包括的なデータセットが、FDAへの提出資料として直接活用可能になる。具体的には以下のリソースを挙げている。
・国立がん研究所(NCI)のSEERプログラム:全米規模のがん登録データ。
・病院システムのデータベース・電子カルテ(EHR)ネットワーク:膨大な実臨床の経過記録。
・保険請求(Claims)データベース:広範な受診歴や処方データ。
これらのリソースは、従来の厳格に管理された臨床試験(RCT)では捉えきれない、多様な人種・年齢層や、複雑な実臨床環境における治療アウトカムを追跡しており、より現実に即した知見を提供するものと期待されている。今後は、提出されたRWEの妥当性や信頼性を、FDAの審査官が「個別の申請案件ごとに」検討していく柔軟な体制へと移行していく。また、医療機器分野での先行導入を受け、FDAは医薬品やバイオ医薬品に関するガイダンスについても、同様の更新を検討する意向を示している。
この政策転換は、デジタルヘルスやAIを活用した医療機器の開発において、極めて大きな意味を持つ。患者のプライバシーを保護しつつ、膨大なリアルワールドデータを規制プロセスに統合できるようになったことにより、開発期間の短縮や、より広範な患者群に対する安全性・有効性の証明が容易になると考えられる。
4. FDA改革③:RWDの品質評価基準を明確化してデータ2次利用を促進
2025年12月18日、FDAは、「医療機器の規制上の意思決定を支援するためのリアルワールドエビデンス(RWE)の活用―業界および米国食品医薬品局職員向けガイダンス」改定版を発行している[7]。これは、2017年の旧版を大幅に更新・刷新するものであり、2022年食品医薬品総合改革法(FDORA)の要請に基づき、最新の技術動向やデータの透明性を反映した内容になっている。
本ガイダンスは、これまで規制承認の障壁となっていた「リアルワールドデータ(RWD)」の品質評価基準を明確にし、その活用範囲を広げることを目的としている。特筆すべき変更点は、FDAが、申請書類における「個人を特定できる患者レベルの機密情報」の提出義務を事実上撤廃したことである。これにより、プライバシーの懸念から活用が難しかった全国規模のがん登録(NCIのSEERなど)、大規模病院のデータベース、保険請求データなどのマクロデータを、規制上の根拠として利用できる道が開かれた。
FDAは、収集されたRWDが「規制上の意思決定に適したエビデンス(RWE)」となり得るかを判断するため、以下の2つの基準で評価する。
・関連性(Relevance):データが検討対象の医療機器や対象疾患、患者集団を十分に代表しているか。重要な変数が含まれ、必要な期間の追跡が可能か。
・信頼性(Reliability):データが正確かつ一貫して収集されているか(Data Accrual)。データの品質管理、監査トレイル、欠損データの処理方法が適切か(Data Integrity)。
本ガイダンスでは、これらを統合的に評価するフレームワークが示されており、スポンサー(申請者)に対し、データの「来歴(Provenance)」と「品質保証計画」の徹底的な文書化を求めている。
また、RWEが利用可能な場面として、以下の通り、具体的な活用シナリオを挙げている。
・承認前申請:通常の市販前届出(510(k))や、市販前承認(PMA)、低リスクで先例のない新製品向けのDe Novo申請 において、主要な臨床エビデンス、あるいは過去の臨床データとしての活用。
・適応拡大:既に承認済みの機器について、新しい用途や対象患者を追加するためのエビデンス。
・市販後調査:承認後の安全性モニタリングや、緊急使用許可(EUA)下で収集されたデータの活用。
・AI/MLの学習:AI・機械学習アルゴリズムのトレーニングや検証用データとしての利用。
さらに、データの透明性を担保し、ガバナンスを強化するために、以下のような新しい推奨事項が含まれている。
・プロトコルの事前策定: 分析を開始する前に解析計画を固め、アウトカムを知った上での「後出し」の解析を避けること。
・IDE(治験機器適用除外): RWD収集のための研究が、いつIDE申請を必要とするかの明確化。通常の診療範囲内でのデータ収集であれば、多くの場合IDEは不要とされる。
・PPRL(プライバシー保護型レコードリンケージ):複数のデータセットを統合する際、患者のプライバシーを保護しつつ高い精度で紐付けを行う技術(PPRL等)の活用を推奨している。
このように、本ガイダンスは、デジタルヘルス時代の要請に応え、「実臨床のビッグデータ」を規制の舞台へ正式に引き上げるための実践的なロードマップとなっている。医療機器製造業者にとっては、臨床試験のコスト削減や期間短縮が期待できる一方、FDAからは従来以上に「データの信頼性」に関する厳格な証明が求められることになる。これは、前述のCMSヘルステクノロジーエコシステムの参画企業が進める「患者主導のデータ統合」の動きを、米国政府が規制面から強力に後押しする内容となっている。
5. FDA改革④:低リスク一般向けウェルネス機器を「医療機器」の対象外に
2026年1月6日、FDAは「一般向けウェルネス: 低リスク機器に関するポリシー―業界および米国食品医薬品局職員向けガイダンス」を発行している[8]。これは、2019年9月27日に発行されたガイダンスの改定版であり、健康的なライフスタイルを促進する製品が、どのような条件を満たせば「医療機器」としての厳格な規制を免除されるかを定義したものである。
本ガイダンスの適用対象となる一般向けウェルネス製品は、以下のいずれかの目的を持つものに限定される。
・第1カテゴリー: 疾患には言及せず、体重管理、フィットネス、ストレス管理、睡眠管理、性的機能などの「一般的な健康状態」を維持・促進するもの。
・第2カテゴリー: 特定の慢性疾患のリスク低減や、疾患と共に「より良く生きる」ための健康的な選択を支援・追跡するもの。
次に、光学式センサー等による非侵襲的な計測(血圧、酸素飽和度、血糖値、心拍変動など)を行う製品については、以下の条件を全て満たす場合に限り、ウェルネス製品と見なされる。
・非侵襲的かつ非植え込み型であること。
・疾患の診断、治療、予防を目的とせず、FDA認可済み医療機器の代替を意図しないこと。
・臨床行為や医学的管理を直接誘導する機能や出力(アラート等)を含まないこと。
・出力値が含まれる場合、メーカーテストや査読済み文献等で妥当性が検証されていること。
そして、以下の要素が含まれる製品は、ウェルネス製品には該当せず、通常の医療機器規制の対象となる。
・診断・治療の標榜: 特定の疾患名や診断閾値への言及、「医療用(メディカルグレード)」、臨床的精度の主張、医療機器の代替となる旨の表明。
・医学的介入: 医学的な管理を要求するアラーム、治療ガイダンス、スクリーニングやモニタリングを目的とした機能。
なお、FDAの規制免除方針は、「低リスク」製品にのみ適用される。製品が「侵襲的」である、「体内に植え込まれる」、あるいは「放射線やレーザー等、規制なしでは安全上のリスクを及ぼす技術」を含む場合は、本ガイダンスの対象外となる。
本ガイダンスは、ウェアラブルデバイス等が収集する高度な生体情報を、医療目的ではなく「健康増進」の範囲に留めるための境界線を明確に引いたものである。製造業者は、ラベル表示や広告がこのウェルネスの範囲を逸脱しないよう厳格に管理することが求められる。
6. FDA改革⑤:臨床意思決定支援ソフトウェアの一部を「医療機器」から除外
加えて2026年1月29日、FDAは「臨床意思決定支援ソフトウェア ― 産業界および米国食品医薬品局職員向けガイダンス」を発行している[9]。本ガイダンスは、21世紀治療法第3060条(a)による連邦食品医薬品化粧品法(FD&C法)の改正に基づき、特定のソフトウェア機能が「医療機器」の定義から除外される基準、およびFDAの規制対象として残る機能についての解釈を明確にすることを目的としている。
本ガイダンスは、医療従事者による使用を意図した臨床意思決定支援(CDS)ソフトウェア機能に適用される。なお、患者や介護者による使用を意図したものを含め、医療機器の定義に該当するソフトウェア機能については、FDA が既に示しているデジタルヘルス関連の方針が引き続き適用されるとしている。
以下の4つの基準(非医療機器CDS基準)をすべて満たすソフトウェア機能は、医療機器の定義から除外される。
1.信号・画像・パターンの処理不可: 体外診断用医薬品からの信号、医用画像、または信号取得システム(生理学的モニタリング等)からのパターンや信号を取得、処理、解析することを意図していないこと。
2.情報の表示・解析・印刷: 患者に関する医療情報、またはその他の医療情報を表示、解析、または印刷する目的で使用されることを意図していること。
3.医療従事者への支援・推奨: 疾病または状態の予防、診断、治療に関して、医療従事者に対して支援または推奨を提供する目的で使用されることを意図していること
4.エビデンスの独立的確認: 医療従事者が、ソフトウェアが提示する推奨のエビデンスを独立して確認できるようにすることを意図しており、個々の患者に対する臨床判断において、当該推奨に主として依拠することを意図していないこと。
本ガイダンスでは、各基準の解釈を助けるために以下のような事例を提供している。
1.医療機器に該当しないCDSソフトウェア機能の例:
2.医療機器に該当しないCDSソフトウェア機能の例― 基準 4 に関するもの
3.医療機器に該当するソフトウェア機能の例:
7. CMSヘルステクノロジーエコシステムから具体化する医療AI
ここまで2025年12月以降にFDAが発表した医療製品規制策を紹介してきたが、前述のCMSのエコシステムを介して、様々な医療AIソリューションが具体化している。表2は、CMSヘルステクノロジーエコシステム主要参画企業のAI関連成果事例を整理したものである。
表2. CMSヘルステクノロジーエコシステム主要参画企業のAI関連成果事例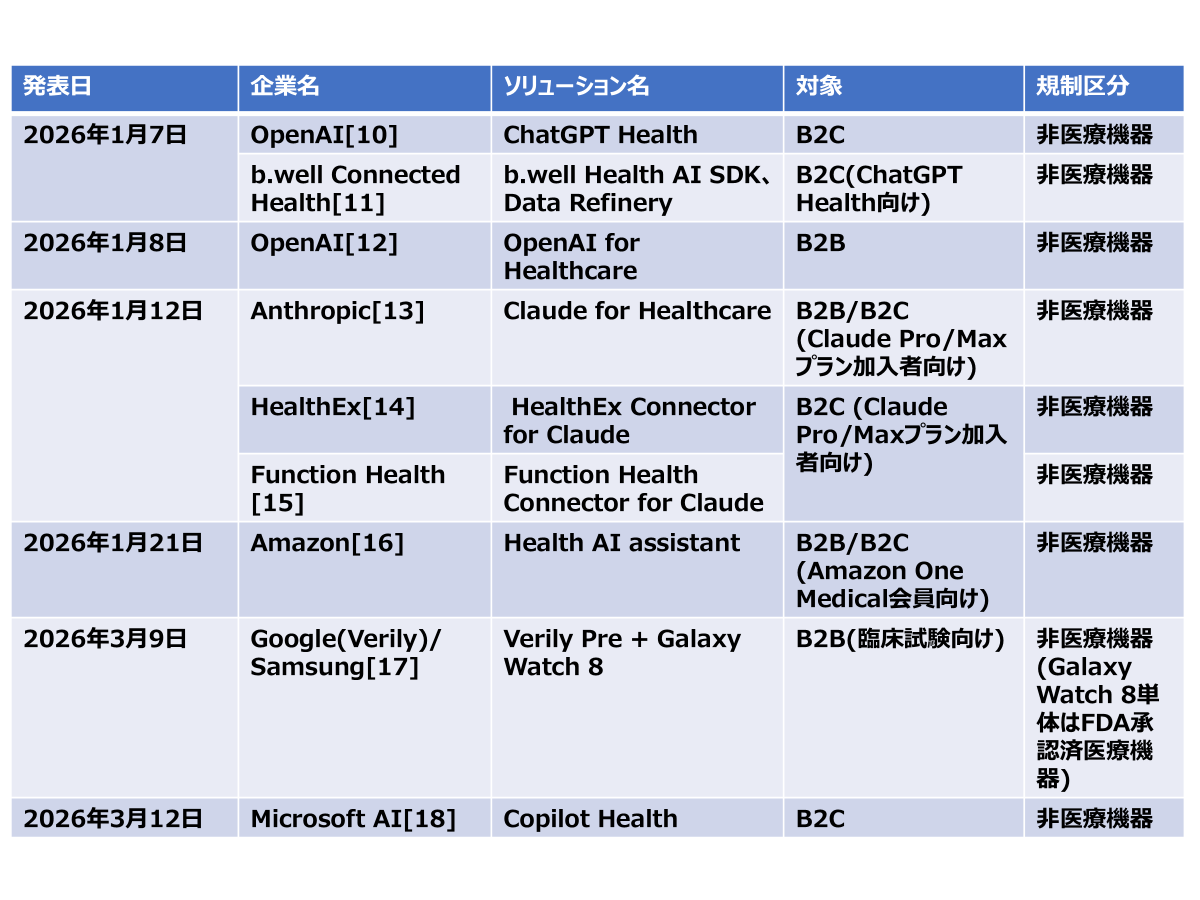
出典:各社プレスリリースを基に筆者作成[10][11][12][13][14][15][16][17][18]
前述のCMSの目標である2026年第1四半期に、OpenAI、Anthropic、Amazon、Google、Microsoftといった米国を代表するビッグテック企業が、続々と医療AIソリューションをリリースしているほか、b.well Connected Health、HealthEx、Function Healthといったヘルスデータ共有・連携ネットワークを支えるビルディングブロック・サプライヤーも登場している。そして注目すべきは、これらの全ソリューションが、FDAの低リスク一般向けウェルネス機器ガイダンスや臨床意思決定支援(CDS)ソフトウェアガイダンスに準拠した「非医療機器」扱いになっている点である。前述の通り、HIPAAプライバシー規則やセキュリティ規則、侵害通知規則そして1974年プライバシー法など、連邦政府および州レベルの法規制を順守することを前提としたCMS相互運用性フレームワーク上で稼働しているが、米国外での利用に際しては、何らかの制限がかかっているケースが多い。
8.非医療機器を所管するFTCの健康侵害通知規則
米国の場合、「医療機器」「非医療機器」に関わらず、デバイスやソフトウェアが、ネットワークを介して、医療施設/医療保険者(CE:Covered Entity)のシステムと連携し、患者の個人データなど保護対象保健情報(PHI:Protected Health Information)をやりとりすれば、HIPAAの適用対象となる。また、PHIに関わるシステム業務やサービスを医療施設/医療保険者から受託する事業者に対しては、事業提携者(BA:Business Associate)としての責務が課せられる。
他方、医療施設/医療保険者やその事業提携者とは無関係に一般消費者が利用するモバイルヘルスアプリケーションやウェアラブル健康機器などの場合、HHSもFDAも所管外となるが、消費者保護の観点から、プライバシー/個人データ保護を所管する米国連邦取引委員会(FTC)が関わってくる。
FTCは、オバマ政権下の2009年8月17日、リーマンショック後の景気浮揚策として制定された「2009年米国再生再投資法(ARRA)」の一部として制定・施行された「健康侵害通知規則」を運用している。具体的には、HIPAAが適用されない個人健康記録(PHR)を提供するベンダーおよび関連するサードパーティアプリケーションを提供する事業者に対して、健康データ侵害を発見したら60日以内(500人以上の個人が影響を受ける侵害の場合は10営業日以内)に、FTCおよび消費者に通知するよう求めていた。
その後2024年7月29日には、改正健康侵害通知規則が発効している[19]。改正規則の主な変更点は、以下の通りである。
1.適用対象の拡大(アプリケーションやウェアラブル機器への適用の明文化)
改正規則では「個人健康記録(PHR)」の定義が明確化され、以下の主体が対象であることが明示された。
・ヘルスケアアプリケーション・フィットネスアプリケーションのベンダー
・スマートウォッチ等の接続デバイス(ウェアラブル)企業
・PHR関連主体(PHRベンダーを介してサービスを提供する企業など)
・サードパーティサービスプロバイダー
2.「侵害」の定義の拡張
従来の「ハッキング等の外部攻撃」だけでなく、「企業による不適切な共有(Unauthorized Disclosure)」も侵害に含まれることが明確化された。
(例)ユーザーの同意なく、広告や分析目的でサードパーティ(Metaのピクセル等)に健康データを送信した場合、それはセキュリティ侵害とみなされ、通知義務が発生する。
3.通知の要件とタイミング
侵害が発覚した場合、以下の相手に通知する必要がある。
・対象となる個人: 500人以上の影響がある場合は、個人への通知と同時かつ最長60日以内
・メディア: 500人以上の影響がある州では、主要なメディアへの公表も必要である。
4.通知方法の近代化
以前は郵便(ファーストクラス)が原則だったが、ユーザーが希望した場合は電子メールでの通知が可能になった。ただし、単なるメール送信だけでなく、アプリ内通知、テキストメッセージ(SMS)、またはウェブサイト上のバナーのいずれかを組み合わせる「2段階の電子通知」が推奨・許可されている。
なおFTCは2015年3月、プライバシー、データセキュリティ、スマートホーム、ビッグデータ、モバイル、IoTなど、次世代技術の消費者保護を目的とした「技術研究・調査室(OTech)」を設置し、その後2023年2月、大幅に機能を拡充・強化した「技術室(OT)」に改組している[20]。
技術室は、以下の3つの柱を通じてFTCを支援している。
・法執行のための調査および措置の強化・支援
・政策および調査イニシアチブに関する、FTC職員および委員会への助言と関与
・最新トレンドの把握と委員会の業務推進に向けた、一般市民および関連専門家との連携
技術室は、セキュリティ、ソフトウェアエンジニアリング、データサイエンス、人工知能(AI)、機械学習、ヒューマンコンピュータインタラクション(HCI)デザイン、およびテクノロジーに関連する社会科学研究に携わるテクノロジストを有しているのが特徴である。特に、プライバシー強化技術(PETs)などの領域で、国立標準技術研究所(NIST)と連携している。
9.おわりに
2000年代後半以降、スマートフォンやクラウドサービスの普及により、個人が手にするテクノロジーの進化スピードが企業のIT投資スピードを追い越す「Consumerization of IT」が起きて、米国の主要ビッグテック企業のプレゼンスが一気に拡大していった。2025年12月以降にCMSヘルステクノロジーエコシステムから生まれた医療AIソリューション群をみると、「Consumerization of Health AI」と言えるような状況が現実化しつつある。その中で、代表的な規制産業であった医療製品業界およびその所管当局は、イノベーションの促進と消費者のデータ保護の両立をどう図っていったらいいのか等々難しい局面に立たされている。米国発の最新医療AI技術は日本にも消費者市場から徐々に参入しつつあり、ガードレール機能の設置等ガバナンス課題の検討が必要となるだろう。
[笹原英司プロフィール]
一般社団法人日本クラウドセキュリティアライアンス・代表理事/関西支部担当
在日米国商工会議所ヘルスケア委員会・副委員長
LinkedIn:https://www.linkedin.com/in/esasahara
宮崎県出身。千葉大学大学院医学薬学府博士課程修了(博士・医薬学)。デジタルマーケティング全般(B2B/B2C)および健康医療/介護福祉/ライフサイエンス業界のガバナンス/リスク/コンプライアンス関連調査研究/コンサルティング実績を有し、Healthtech/Medtechスタートアップ向けにクラウドネイティブセキュリティに関する啓発活動を行っている。
(脚注)
[i] アプリ同士をつなぐ役割を果たす
[ii] 実際の医療現場や日常生活で得られる医療・健康データの総称
(参考文献)
[1] Centers for Medicare & Medicaid Services (CMS), “White House, Tech Leaders Commit to Create Patient-Centric Healthcare Ecosystem”, July 30, 2025.
https://www.cms.gov/newsroom/press-releases/white-house-tech-leaders-commit-create-patient-centric-healthcare-ecosystem
[2] Office of the Assistant Secretary for Technology Policy (ASTP) / Office of the National Coordinator for Health IT (ASTP/ONC), “United States Core Data for Interoperability (USCDI)”, as of March 16, 2026
https://isp.healthit.gov/united-states-core-data-interoperability-uscdi
[3] HL7 Foundation, “US Core Implementation Guide”, as of March 16, 2026
https://build.fhir.org/ig/HL7/US-Core/
[4] Centers for Medicare & Medicaid Services, “Health Technology Ecosystem > Early Adopters”, As of July 30, 2025
https://www.cms.gov/health-tech-ecosystem/early-adopters
[5] U.S. Food and Drug Administration (FDA), ” FDA Launches TEMPO: A First-of-Its-Kind Digital Health Pilot to Expand Access to Chronic Disease Technologies ”, December 5, 2025
https://www.fda.gov/news-events/press-announcements/fda-launches-tempo-first-its-kind-digital-health-pilot-expand-access-chronic-disease-technologies
[6] U.S. Food and Drug Administration (FDA), ” FDA Eliminates Major Barrier to Using Real-World Evidence in Drug and Device Application Reviews ”, December 15, 2025
https://www.fda.gov/news-events/press-announcements/fda-eliminates-major-barrier-using-real-world-evidence-drug-and-device-application-reviews
[7] U.S. Food and Drug Administration (FDA), ”Use of Real-World Evidence to Support Regulatory Decision-Making for Medical Devices— Guidance for Industry and Food and Drug Administration Staff”, December 18, 2025
https://www.fda.gov/regulatory-information/search-fda-guidance-documents/use-real-world-evidence-support-regulatory-decision-making-medical-devices
[8] U.S. Food and Drug Administration (FDA), ” General Wellness: Policy for Low Risk Devices — Guidance for Industry and Food and Drug Administration Staff”, January 6, 2026
https://www.fda.gov/regulatory-information/search-fda-guidance-documents/general-wellness-policy-low-risk-devices
[9] U.S. Food and Drug Administration (FDA), ”Clinical Decision Support Software — Guidance for Industry and Food and Drug Administration Staff ”, January 29, 2026
https://www.fda.gov/regulatory-information/search-fda-guidance-documents/clinical-decision-support-software
[10] OpenAI, “Introducing ChatGPT Health — A dedicated experience in ChatGPT designed for health and wellness”, January 7, 2026
https://openai.com/index/introducing-chatgpt-health/(表2内)
[11] b.well Connected Health, “OpenAI Selects b.well to Power Secure Health Data Connectivity for AI-Driven Health Experiences in ChatGPT”, January 7, 2026
https://www.prnewswire.com/news-releases/openai-selects-bwell-to-power-secure-health-data-connectivity-for-ai-driven-health-experiences-in-chatgpt-302655598.html(表2内)
[12] OpenAI, “Introducing OpenAI for Healthcare”, January 8, 2026
https://openai.com/index/openai-for-healthcare/(表2内)
[13] Anthropic, “Advancing Claude in healthcare and the life sciences”, January 12, 2026
https://www.anthropic.com/news/healthcare-life-sciences(表2内)
[14] HealthEx, “HealthEx Partners with Anthropic to Turn Patients’ Scattered Medical Records into Actionable Health Insights”, January 11, 2026
https://www.healthex.io/press/healthex-anthropic-partnership(表2内)
[15] Function Health, “Function Launches Integration with Claude, Powered by Anthropic”, January 12, 2026
https://www.prnewswire.com/news-releases/function-launches-integration-with-claude-powered-by-anthropic-302658537.html(表2内)
[16] Amazon, “Amazon One Medical introduces agentic Health AI assistant for simpler, personalized, and more actionable health care”, January 21, 2026
https://www.aboutamazon.com/news/retail/one-medical-ai-health-assistant(表2内)
[17] Verily, “Verily and Samsung Collaborate to Accelerate Clinical Research with the Galaxy Watch and Pre Platform”, March 9, 2026
https://verily.com/perspectives/verily-and-samsung-collaborate-to-accelerate-clinical-research-with-the-galaxy-watch-and-pre-platform(表2内)
[18] Microsoft AI, “Introducing Copilot Health”, March 12, 2026
https://microsoft.ai/news/introducing-copilot-health/(表2内)
[19] Federal Trade Commission, “16 CFR Part 318: Health Breach Notification Rule”, May 30, 2024
https://www.ftc.gov/legal-library/browse/federal-register-notices/16-cfr-part-318-health-breach-notification-rule
[20] Federal Trade Commission, “Office of Technology”, as of March 16, 2026
https://www.ftc.gov/about-ftc/bureaus-offices/office-technology

