R-2022-021
| 1 背景 2 方法 2.1 日本財団PCR検査事業登録施設の特徴とグループ分類 2.2 マルコフモデルの設定と仮定 2.3 費用対効果分析 2.4 感度分析 3 結果 4 考察 5 結論 |
1 背景
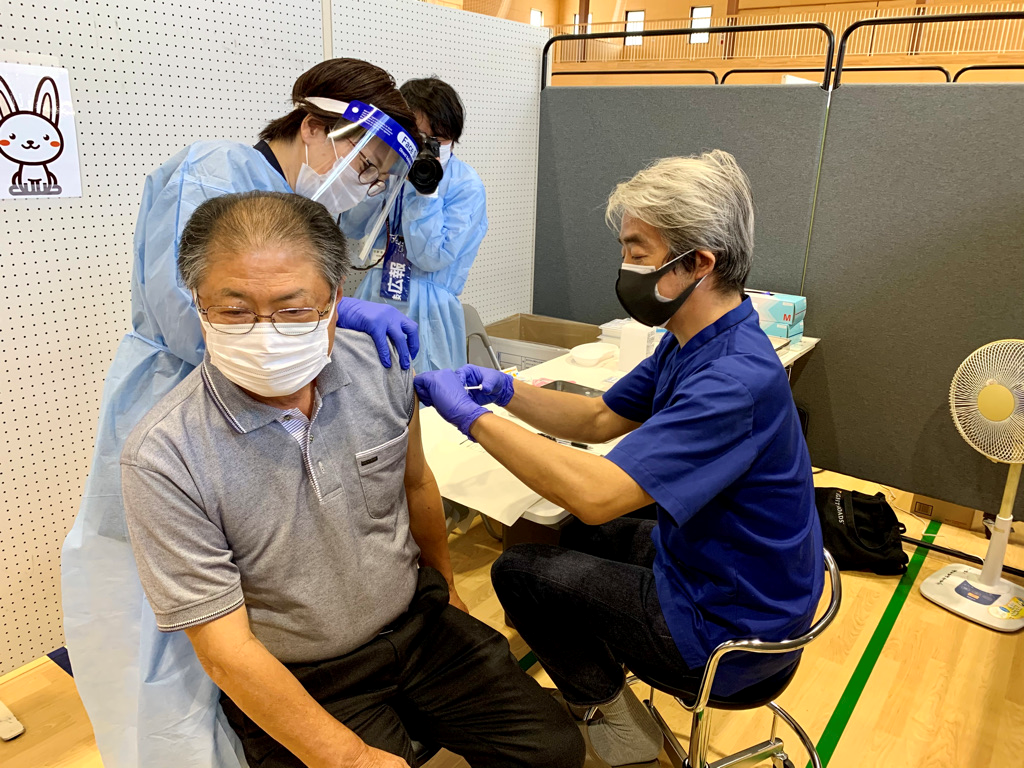
新型コロナウイルス(COVID-19)流行期において、高齢者向け施設・事業所に勤務するエッセンシャルワーカーに対して感染伝播対策としての定期PCR検査を行うことは、施設内の集団感染を防止し、業務体制を維持し、ひいては社会経済活動継続に貢献すると考えられる。諸外国では、パンデミック初期から医療・介護施設において定期的にPCR検査が実施されてきた[1][2][3][4]。
日本において、PCR検査は行政検査の枠組みの一環として医師の判断の下で行うことが基本であり、スクリーニング(健康な人も含めた集団から特定疾患の発症者や発症が予測される人を選別する医学的手法)を目的としてPCR検査を拡大することには極めて消極的であった。また、「コストパフォーマンス」の観点からPCR検査拡大を懸念する意見もあった[5]。
今後のパンデミック下における予防対策を検討する上で、定期PCR検査を実施することの有効性を科学的かつ実証的に評価することは極めて重要である。本稿では、日本財団が関東圏の高齢者施設で行った定期PCR検査事業の実際のデータを活用し、費用対効果分析を行った結果について考察を行う。なお、検査の社会的意義および課題についてはこちらのReviewを参照されたい。
2 方法
2.1 日本財団PCR検査事業登録施設の特徴とグループ分類
本分析では、2021年3月1日~2022年4月30日に、日本財団PCR検査事業に登録した関東4都県(東京、埼玉、千葉、神奈川) の11,706の高齢者施設のデータを活用した。同PCR検査事業は施設単位で申し込みができ、原則、無症状の職員全員を対象に、上限週1回までの頻度で定期検査を行うことが可能であった。
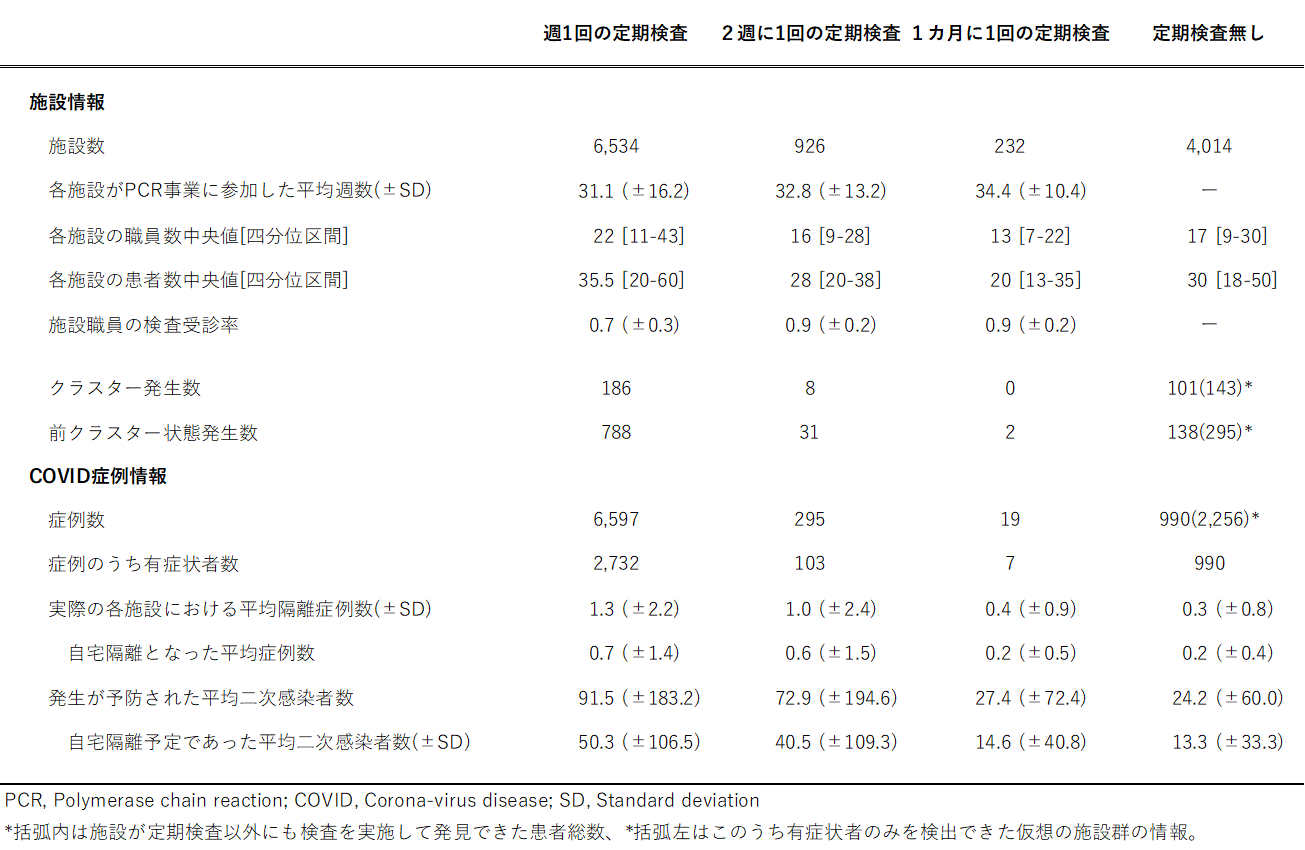
PCR検査事業に登録した施設を、7割以上の参加期間において、①週1回の定期PCR検査を行った施設、②2週に1回の定期PCR検査を行った施設、③1カ月に1回の定期PCR検査を行った施設の3種類のグループに分類した。また、①~③のグループに分類されなかった施設のデータを用いて、④検査を行っていない仮想上の施設のグループを比較対象として作成した(表1)。
表1:定期PCR検査の頻度にて分類された高齢者施設の特徴
2.2マルコフモデルの設定と仮定
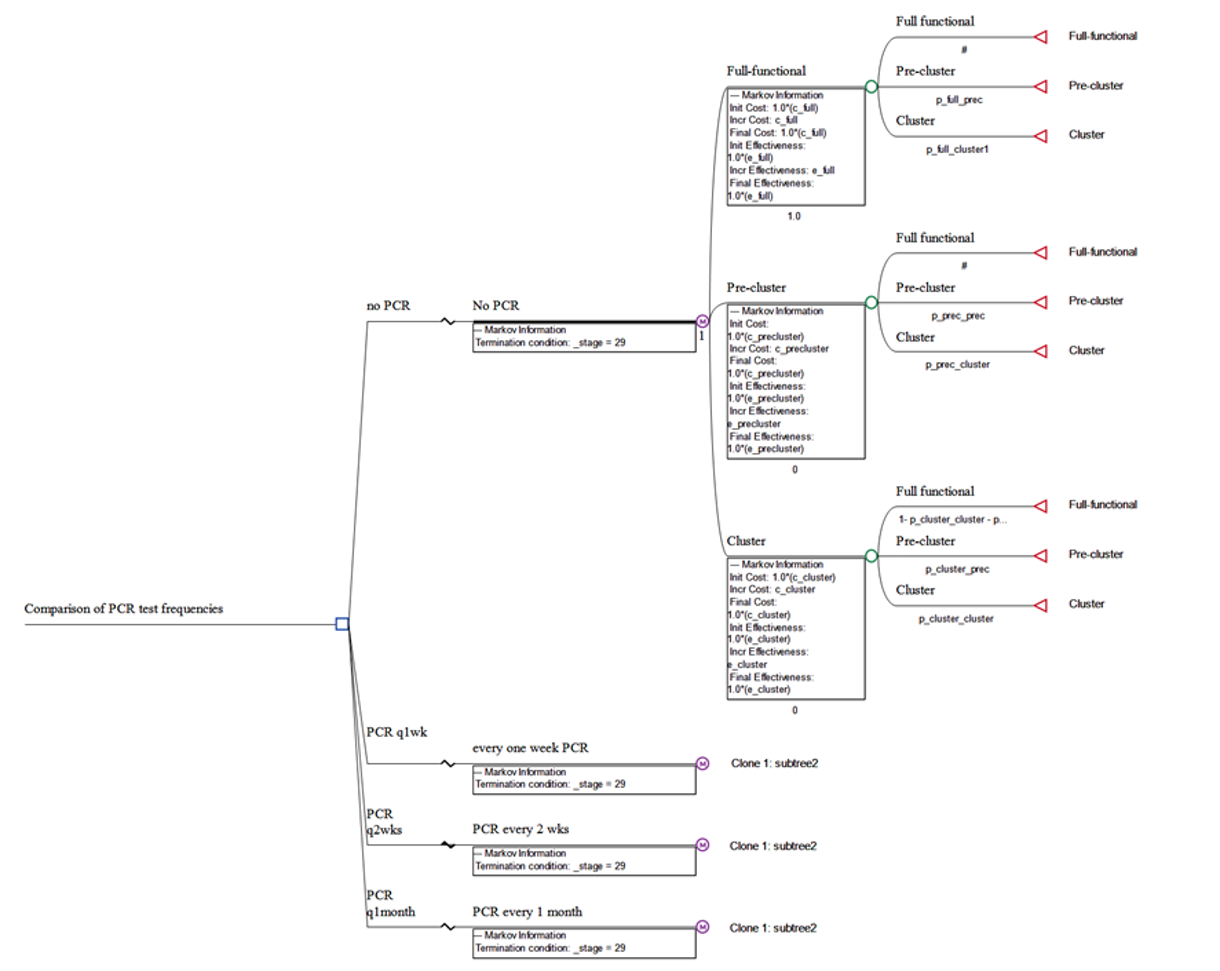
COVID-19感染拡大のシミュレーションには、日本財団のPCR検査事業に登録した施設の機能が、感染の発生状況により、毎週、クラスター状態、前クラスター状態、通常機能状態の間を移行する可能性があることを基本とするマルコフモデルを用いた(図1)。
図1:マルコフモデルにおける施設間の遷移
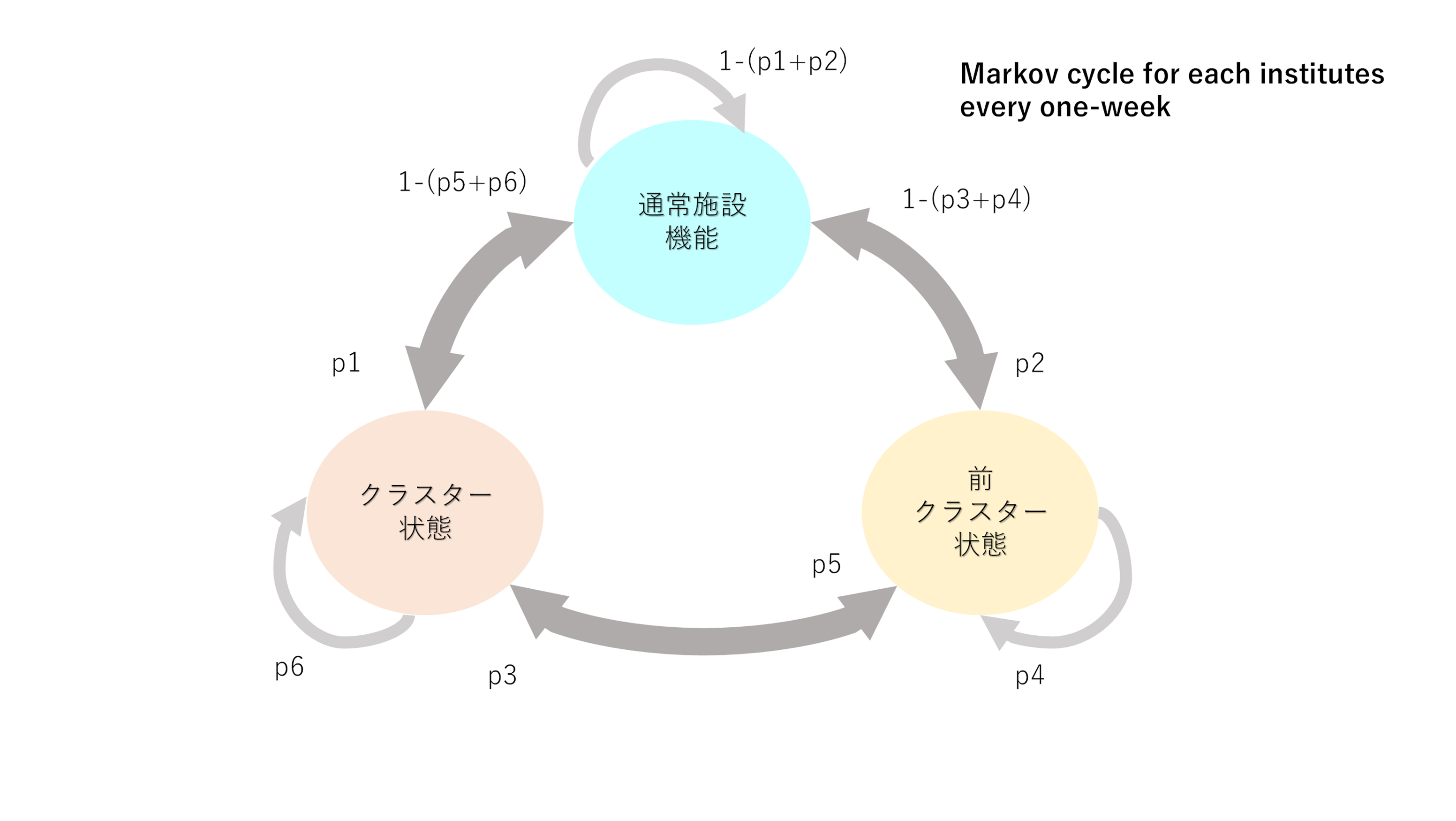
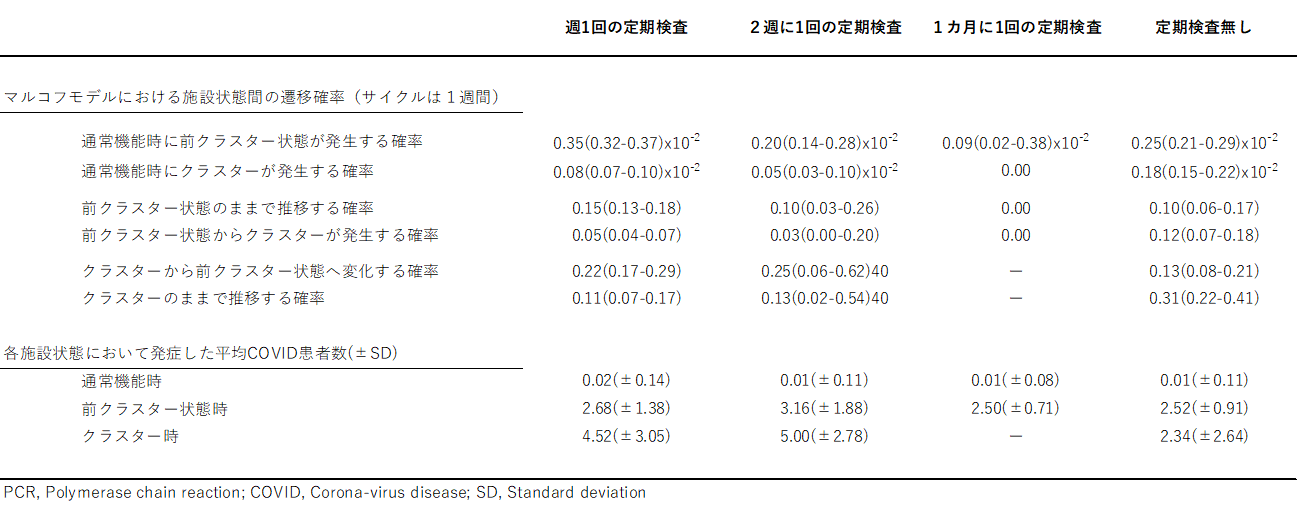
施設におけるクラスター発生は、1日に5人以上の陽性者が確認された、もしくは施設全体の15%以上の職員が陽性となった場合と定義した[6]。また、前クラスター状態は、1日に2~4人の陽性者が確認された、もしくは施設全体の5~14%の職員が陽性となった場合と定義した[7][8]。1日に0~1人の陽性者が確認された、もしくは施設全体の5%未満の職員が陽性であった場合、施設は通常機能状態とした。他方、施設の状態(クラスター、前クラスター、通常機能)に応じて、職員もしくは入居・利用者の間で感染が確率的に発生すると設定とした。施設機能が変化する確率や、感染者発生数の確率は、実データを参考にして割り当てた(図2、表2)。
図2:各施設の遷移状態を示すマルコフモデルの決断樹
表2:マルコフモデルにおける施設状態間の遷移確率と各施設状態におけるCOVID発症の頻度
マルコフモデルにおいては、次の通り仮定した。(1)マルコフモデルにおける施設状態間の移行確率はパンデミック期間を通じて一定である。(2)施設間でCOVID患者の発生確率は独立している。(3)PCR検査の感度は、既存のデータを基に91.4%を最頻値として、80~100%の分布を取る[9][10]。(4)感染者は、10~14日間の感染期間中にPCR検査が陽性となる。(5)感染者のうち、40~70%(最頻値 58%)が無症状である[11]。(6)PCR検査の頻度によって同定できる無症状者の割合は変化し、①週1回の検査を行った施設は80~100%、②2週に1回の検査を行った施設は70%、③1カ月に1回の検査を行った施設は50%の割合である[4]。(7)各施設はCOVID流行の恐れがあると判断した時期に検査事業に参加する。(8)PCR検査の頻度によって施設職員の受検率が異なり、①週1回の検査を行った施設は平均70%、②2週に1回の検査を行った施設は平均87%、③1カ月に1回の検査を行った施設は平均90%の割合で受検した。(9)感染予防意識の高い高齢者施設職員であるため、感染症状がある者は全員速やかに自主隔離をする。(10)自主隔離を行った際にも隔離費用は発生する。(11)感染者のうち、20~100%(最頻値 50%)が自宅での経過観察となる。(12)隔離患者のうち2.5~30%の患者が入院治療を必要とする。
上記の設定により、各施設が職員を対象に定期PCR検査を行い、検査によりCOVID陽性者が判明し、陽性者の発生数により施設機能が変化するというマルコフモデルのシミュレーションを行った。さらに、モンテカルロ・シミュレーション手法を用いることで、勤務者数や入居・利用者数が異なる全ての施設に対して前述のシミュレーションを行い、パンデミック下の高齢者施設における定期PCRの費用対効果と同検査の適切な頻度を推定した[11]。なお、すべてのパラメータは、分布内の数値が各施設にランダムに割り振られる設定とした。解析ソフトはTreeAge Pro Healthcare 2022 R1.2を使用した。
2.3 費用対効果分析
マルコフモデルを基にモンテカルロ・シミュレーションを行い、職員に対して定期PCR検査を実施した高齢者施設が必要とした費用と削減できた費用をPCR検査の頻度で分類したグループ①~④の間で比較した。費用分析における費用についての内訳は表3の通りである。
表3:費用分析において用いたPCR実施頻度毎の必要費用と削減費用の構成
定期PCR検査を実施した高齢者施設が必要とした費用には、(1)PCR検査費用、(2)隔離費用、(3)隔離施設で患者を見守るスタッフに支払う給与、(4)入院・外来治療にかかる費用を含めた。
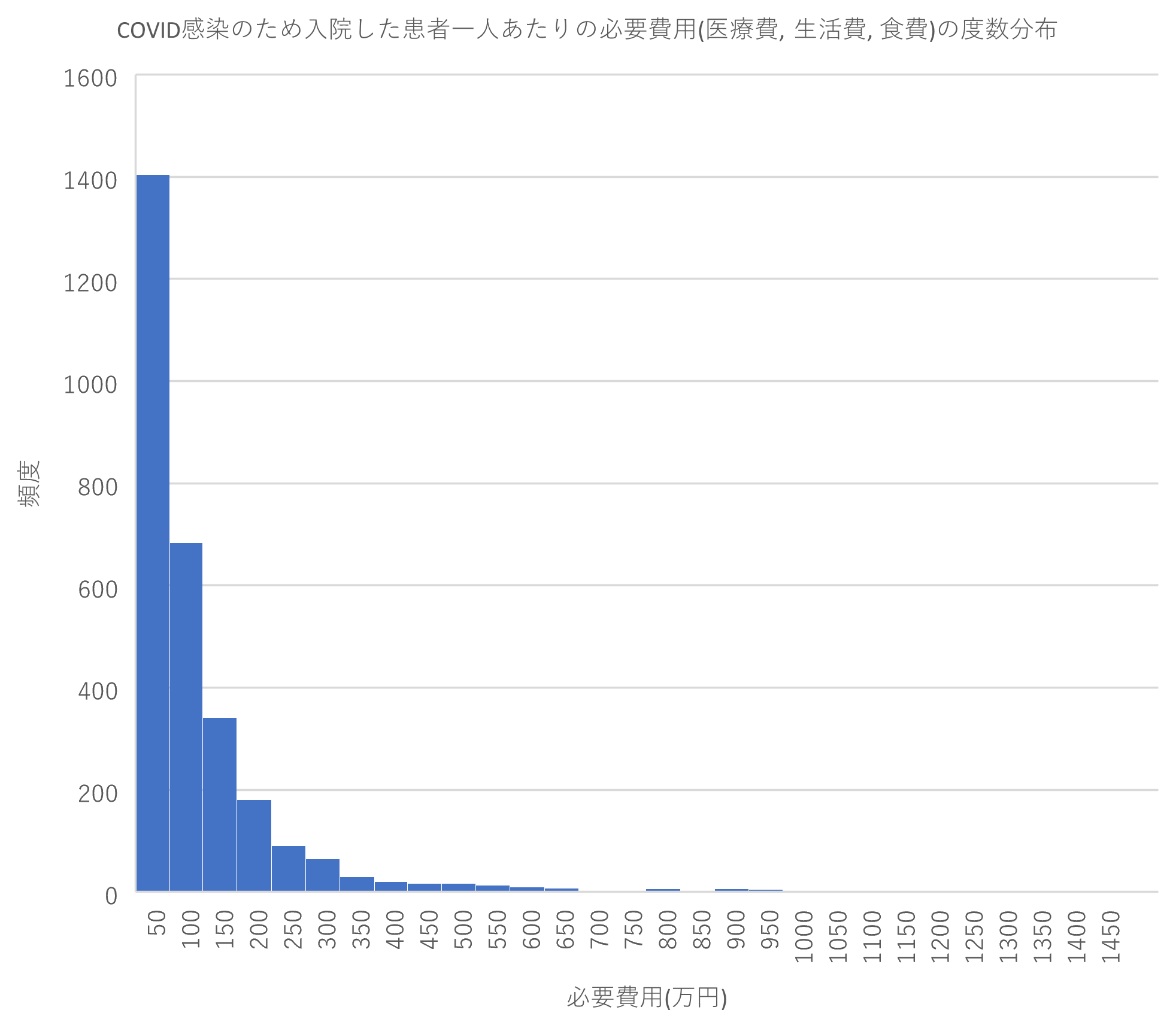
PCR検査費用の基本設定は、日本財団のPCR検査事業で実際に用いられた1件あたりの費用1,600~2,300円を参考に、1,500~3,000円と設定した。隔離のために必要な施設費用は、文献による情報と体制の変化に伴う費用の低下を考慮した上で、1日当たり10,000~20,000円と設定した[12]。隔離施設に入所した患者を見守るスタッフにかかる給与は、20~40人の患者に対して、医師と看護師一人ずつの支払いが発生すると仮定し、医師の時給は15,000~25,000円、看護師の時給は1,500~2,500円と設定した。COVID患者の治療費については、入院率を0.02~35%とし [13](図3、表4)、急性期公立病院におけるCOVID患者の治療費用(入院費用と退院後外来費用)の実際の分布(超指数分布, ラムダ1.1×10-6, p 0.065, 平均値 92万4500円)をモデルに導入した(図4)。
図3:東京・神奈川・埼玉・千葉におけるCOVID陽性者数、陽性者の入院率、入院患者の重症化率、陽性者の自宅隔離率の推移
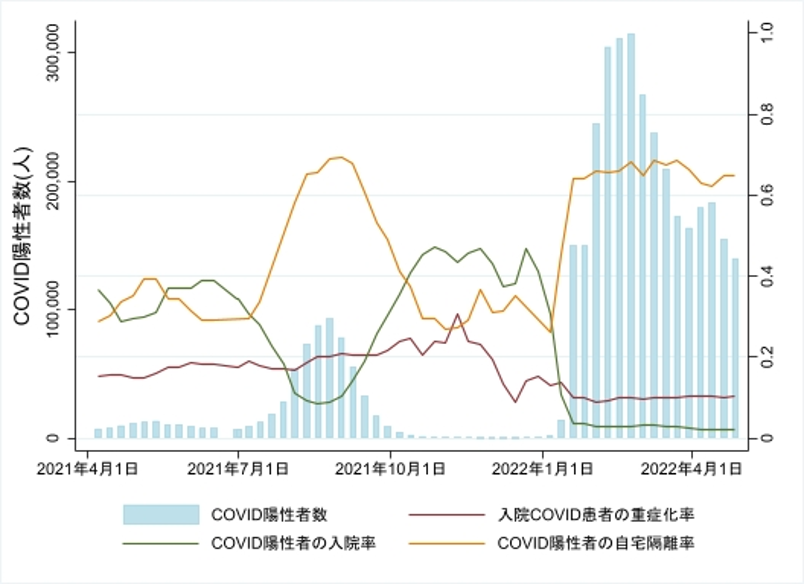
表4:高齢者施設が日本財団PCR検査事業参加期間中に予防できた二次感染者数と必要費用・削減費用の比較
図4:COVID感染のため入院した患者一人あたりの治療費用の度数分布
定期PCR検査を実施した施設が削減できた保健アウトカム上の効果および費用を算出するため、まず初めに発生を予防できた感染者数を算出した。発生を予防できた感染者数は、集団を感受性(Susceptible)、潜伏期(Exposed)、感染(Infectious)、回復(Recovered)の4種類に区分するSEIRモデルを用い、最終規模方程式、ワクチン効果による発生予防効果も考慮して算出した[10]。発生が予防できた感染者数の推定式は、(1-ワクチン効果)×(感染する可能性がある人数)×(最終規模)-(実際の感染者数) と設定した。ワクチン効果は、ワクチンにより感染症発症を予防できる確率として0から1の値を取り得るとした。最終規模を算出する方程式の詳細は、次の通りである。
最終規模方程式
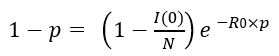
p :最終的に感染を経験する個人の割合
I (0) :0時点での感染者の数
N :感染を経験する可能性のある人数
R0 :基本再生産数
マルコフモデルにおける各施設の機能において、施設で発生したCOVID感染者数と、感染の可能性がある人数(職員と入所・利用者数)を、前記の感染数推定式に入力することにより、発生を予防できた患者数の推定値を算出した。また、発生を予防できた感染者数のうち、(1)無症状の感染者から発生した2次感染者を隔離するために必要であったはずの費用、(2)隔離施設において患者を見守るスタッフに支払うはずであった給与、(3)感染者のうち入院した患者への治療費用を削減できた費用とした。なお、費用に関するパラメータも、分布内の数値が各施設にランダムに割り振られる設定とした。
2.4 感度分析
費用対効果の基本分析に加え、COVID患者の入院率、PCR検査費用、ワクチン効果(ワクチンが感染者を減らす割合)、無症状率、PCR検査感度の5要素について感度分析を行い、定期PCR検査の頻度によって分類したグループ間の優位性への影響を評価した。感度分析のパラメータも、分布内の数値が各施設にランダムに割り振られる設定とした。
3 結果
費用対効果分析に用いるマルコフモデルを作成するため、日本財団が集積した延べ 7,604,463件のPCR検査受付データと10,645人のCOVID感染者(9,392人は初回感染確定者)に関するデータを用いた。9,392人のCOVID初回感染確定者のうち、男性が32.2%、88.8%に2回のワクチン接種歴、65.8%に3回のワクチン接種歴があった。日本財団のPCR検査は、原則として無症状の職員が対象であったが、実際にはCOVID感染確定者の41.9%が有症状であった。
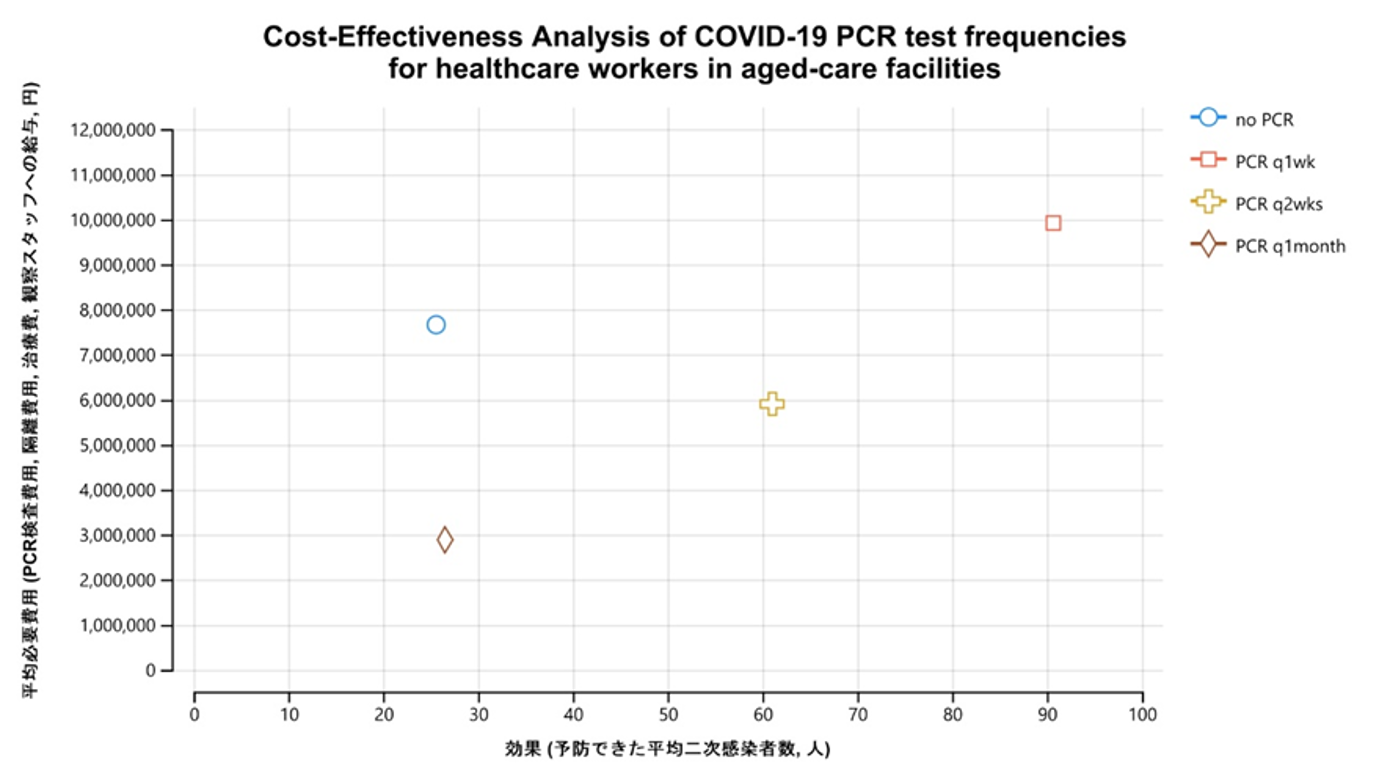
図5と表4は高齢者施設が必要とした費用と予防できた二次感染者数の費用対効果分析の結果を表している。図5のY軸は定期PCR検査を実施した施設が必要とした費用、X軸は予防できた二次感染者数を示している。1カ月に1回定期検査を行った施設は、定期検査を行わなかった施設と比較し、若干多くの二次感染者を予防し、必要費用は38%程度に抑えた。2週に1回定期検査を行った施設は、定期検査を行わなかった施設の77%の費用で、2.4倍の二次患者を予防した。週1回定期検査を行った施設は、定期検査を行わなかった施設より約30%多くの費用を必要としたが、3.5倍の二次患者を予防できたため、費用対効果は高かった。
図5:高齢者施設職員へのPCR検査実施体制の費用対効果分析
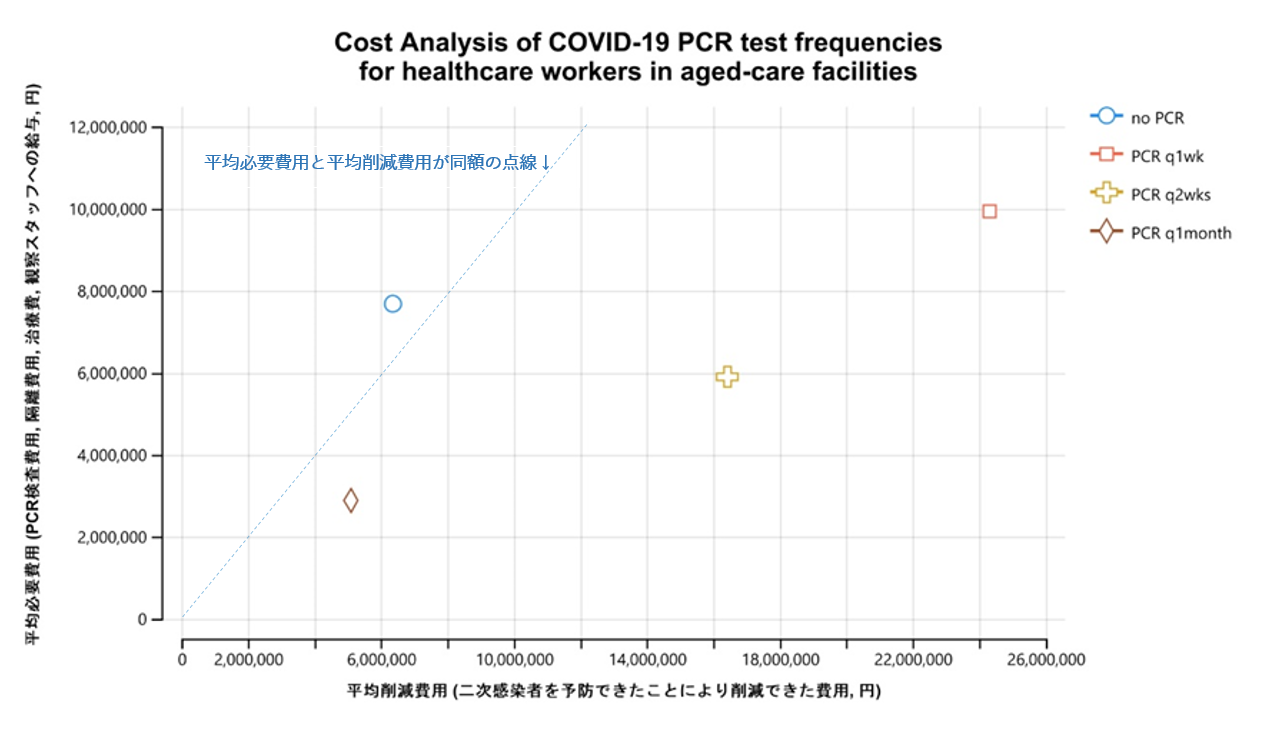
図6と表4は高齢者施設が必要とした費用と削減できた費用を表している。図6の斜破線は平均必要費用と平均削減費用が同額になるラインを示しており、斜破線の左上は必要費用が削減費用を上回り、右下は削減費用が必要費用を上回ることを意味している。左上に交点があるのは定期PCR検査を実施しなかった施設のみであり、定期検査を実施したすべての施設の交点が右下にあることから、頻度にかかわらず、定期検査を実施したすべての施設で削減費用が必要費用を上回ったことがわかる。
図6:高齢者施設職員へのPCR検査実施体制の費用分析
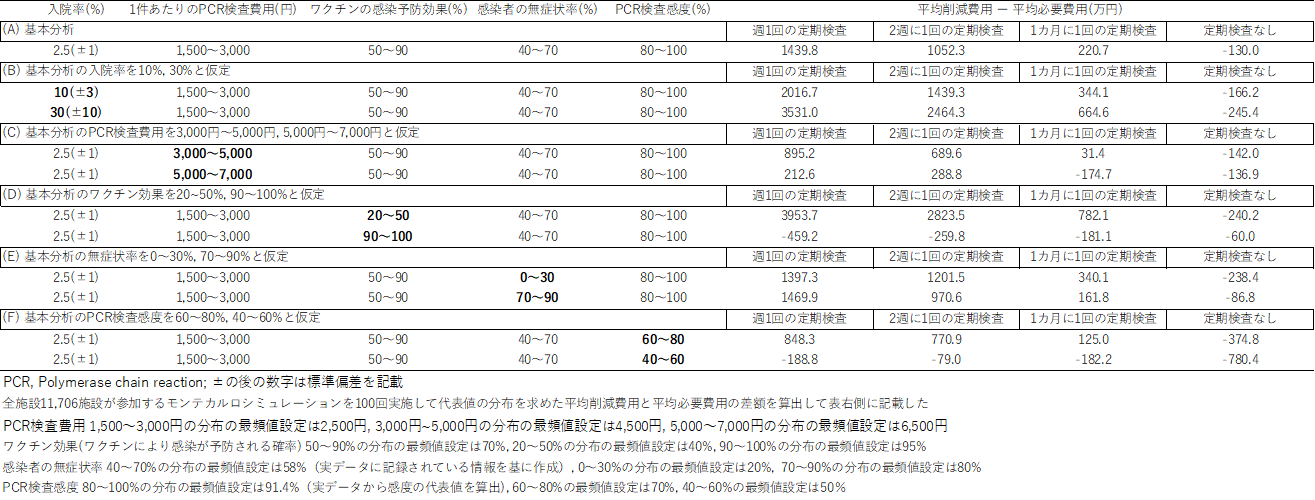
表5は感度分析の結果を表している。COVID感染者の入院率が高いとき、定期PCR検査を行う施設では、削減費用が顕著に増加した。一方で、定期PCR検査を行わない施設では必要費用が増加した。また、入院率が高いとき、検査頻度は高い方が費用削減効果は高くなった。1件あたりのPCR検査費用が高額になると、定期PCR検査を行う施設では必要費用が増加し、削減できた費用との差額が減少した。特に、PCR検査費用が5,000~7,000円の場合、1カ月に1回定期検査を行う施設では必要費用が削減費用を上回り、その損失額は定期検査を行わない施設より高くなった。また、週1回定期PCR検査を行う施設より、2週に1回定期PCR検査を行う施設の方が、費用の削減効果が高かった。COVID感染者の無症状率が高いとき、週1回定期PCR検査を行う施設では唯一基本分析より削減費用が高く、その他の施設では削減費用が低くなった。ワクチン効果(ワクチンにより感染を予防できる効果)が高いとき、およびPCR検査感度が低いときは、すべての施設において必要費用が削減費用を上回った。
表5:費用分析におけるCOVID感染者の入院率とPCR検査費用についての感度分析
4 考察
日本財団のPCR検査データを活用したシミュレーション分析によると、パンデミック下の高齢者施設における定期PCR検査は、週1回、2週に1回、月1回のいずれの頻度で行った場合においても、定期検査を行わなかった施設と比較して、より多くの二次感染者を予防でき、その結果、感染症対策にかかる総費用を削減できることが示唆された。
感度分析の結果からは、感染症の特性および関連する各種条件によって、費用削減効果は異なるが、全体として結論に大きな変化は見られなかった。COVID感染者の入院率が高いとき、定期PCR検査の費用削減効果が最も高くなる。これは入院治療費にかかる費用は高額であり、定期PCR検査を行う施設では入院治療費が削減費用となるためである。一方で、定期PCR検査を行わない施設では、入院治療費が必要費用となるため、損失額が更に膨らむ。入院率とCOVID感染者の無症状率が高いときは、定期PCR検査の頻度が高い方(週1回)が費用削減効果は高い。これは、定期PCR検査を頻回に行うことで、無症状の患者から発生するより多くの二次患者を予防でき、彼らに必要となる高額な入院治療費を削減できるためである。一方、PCR検査費用が高額(5,000~7,000円)であるとき、1カ月に1回の定期検査に費用削減効果は期待できない。また、週1回よりも2週に1回の検査の方が費用対効果は高いと考えられる。この結果は、諸外国の高齢者施設のような二次感染リスクの高い環境において推奨された結果と類似する[4]。PCR検査費用が高額である場合、定期検査の実施およびその頻度について熟慮する必要がある。一方、ワクチン効果が高いとき、またPCR検査の感度が低いときは、定期PCR検査を行う意義について再考すべきである。
PCR検査費用が高額である場合、検査体制の長期維持にとって負担になる可能性があるため、PCR検査の代替となる安価で迅速な抗原検査キットへの切り替えも検討すべきである。ただし、検査による診断能力には差があるため、抗原検査キットの疾患同定率に関する評価および費用対効果分析が必要である。2022年4月に高齢者施設の職員を対象とした検査を週1回のPCR検査から週2回の抗原検査に切り替えた地域がある[15]。早期に適切な検査体制に移行することは、医療資源の適切な分配のみならず、パンデミックからの復興も促すと考えられる。
本稿の解析は、実際のデータを基にしているという強みがあるものの、現実を簡略化したモデル分析であるため、解釈には注意が必要である。
5 結論
本稿の分析では、パンデミック下の高齢者施設職員への定期PCR検査は、無症状感染者から発生する二次感染者を予防し、二次感染患者の治療等に必要となる費用を抑制することができるため、費用対効果が高いという結果が得られた。ただし、ウイルスの特性等による患者の症状の有無、入院率、ワクチン効果、流通する検査の時価や感度等に鑑み、定期PCR検査の必要性と適切な頻度について随時適切な判断を行うことが肝要である。長期的には、安価で高い利便性を持つ抗原検査キットとの組み合わせ等、持続可能な検査体制の確立が求められている。
本件に関する定性的調査分析はこちらをクリックください
[1] Kimball, A., Hatfield, K. M., Arons, M., CDC COVID-19 Investigation Team (2020). Asymptomatic and Presymptomatic SARS-CoV-2 Infections in Residents of a Long-Term Care Skilled Nursing Facility - King County, Washington, March 2020. MMWR. Morbidity and mortality weekly report, 69(13), 377–381.
[2] Ladhani, S. N., Chow, J. Y., Janarthanan, R., London Care Home Investigation Team (2020). Increased risk of SARS-CoV-2 infection in staff working across different care homes: enhanced CoVID-19 outbreak investigations in London care Homes. The Journal of infection, 81(4), 621–624.
[3] Holmdahl, I., Kahn, R., Hay, J. A., Buckee, C. O., & Mina, M. J. (2021). Estimation of Transmission of COVID-19 in Simulated Nursing Homes With Frequent Testing and Immunity-Based Staffing. JAMA network open, 4(5), e2110071.
[4] Chin, E. T., Huynh, B. Q., Chapman, L., et al. (2021). Frequency of Routine Testing for Coronavirus Disease 2019 (COVID-19) in High-risk Healthcare Environments to Reduce Outbreaks. Clinical infectious diseases: an official publication of the Infectious Diseases Society of America, 73(9), e3127–e3129.
[5] 橋本佳子, (2020年10月10日). PCR検査で本庶氏と西浦氏が激論、京大が新型コロナ緊急シンポ
https://www.m3.com/news/open/iryoishin/830556?category=opinion
[6] Furuse, Y., Sando, E., Tsuchiya, N., et al. (2020). Clusters of Coronavirus Disease in Communities, Japan, January-April 2020. Emerging infectious diseases, 26(9), 2176–2179.
[7] Ariza-Heredia, E. J., Frenzel, E., Cantu, S., Carlson, M., et al. (2021). Surveillance and identification of clusters of healthcare workers with coronavirus disease 2019 (COVID-19): Multidimensional interventions at a comprehensive cancer center. Infection control and hospital epidemiology, 42(7), 797–802.
[8] Ashswita Ravindran, 2021, 93% Active Covid Clusters’ Positivity Rate Above 5%, https://codeblue.galencentre.org/2021/01/18/93-active-covid-clusters-positivity-rate-above-5/
[9] Hamra, G., MacLehose, R., & Richardson, D. (2013). Markov chain Monte Carlo: an introduction for epidemiologists. International journal of epidemiology, 42(2), 627–634.
[10] Ifguis, O., El Ghozlani, M., Ammou, F. (2020). Simulation of the Final Size of the Evolution Curve of Coronavirus Epidemic in Morocco using the SIR Model. Journal of environmental and public health, 2020, 9769267.
[11] Hamra, G., MacLehose, R., & Richardson, D. (2013). Markov chain Monte Carlo: an introduction for epidemiologists. International journal of epidemiology, 42(2), 627–634.
[12] 兪 炳匡, 高木 俊, 野口 晴子, (2020) 新型コロナウイルスの無症状者に対するPCR 検査の費用対便益分析, Oct 2020. WINPEC Working Paper Series No. J2002. https://www.waseda.jp/fpse/winpec/assets/uploads/2020/10/J2002-1_version_p6_corrected.pdf
[13] 厚生労働省, 2022年6月 療養状況等および入院患者受入病床数等に関する調査についてhttps://www.mhlw.go.jp/stf/seisakunitsuite/newpage_00023.html
[14] Du, Z., Pandey, A., Bai, Y., et al. (2021). Comparative cost-effectiveness of SARS-CoV-2 testing strategies in the USA: a modelling study. The Lancet. Public health, 6(3), e184–e191.
[15] Public Health Agency, Belfast Ireland, Testing in care homes and hospices (including visitor and care partner testing) April 2022. https://www.publichealth.hscni.net/covid-19-coronavirus/guidance-hsc-staff-healthcare-workers-and-care-providers/testing-care-homes