このレビューのポイント
・今回、ワクチン接種と自然感染の双方によるハイブリッド免疫の減衰と再感染を考慮できる数理モデルを用いて、2023年5月1日現在のCOVID-19の国内の集団免疫レベルの推計を行った。
・第8波後の2023年2月から国内の集団免疫レベルは減少傾向にあるという推計結果が得られた。この推計結果は、2022年11月および2023年2月に実施された抗体検査とほぼ合致している。
・今後集団免疫レベルが低下したタイミングで再流行(第9波)が起こる可能性は十分考えられるが、自然感染やハイブリッド免疫による重症化予防効果は長期間持続するため、重症者数と死亡者数は第8波以上には増えないことが予想される。しかし、全体の感染者数が増えればハイリスク群への感染が増え、重症者数と死亡者数(特に間接死亡)が増えるリスクがある。
・ワクチン接種率が低く自然感染例の少ない小児の間で感染が拡大すれば、外来機能が逼迫し、全体の医療に影響を与える恐れがある。
・5類移行後も詳細な分析を続けるためには、各地域の検体陽性率、重症率、致死率、病原体の把握等、必要なデータを限定し、医療機関に負荷のかからない方法で、頻繁かつ確実にデータ収集を行うことが重要である。
R-2023-009
1.はじめに
2023年5月1日現在、新型コロナウイルス感染症(COVID-19)の国内における1週間当たりの新規感染者報告数は、第8波(2022年10月~2023年1月)のピーク時の約5%という低い水準に保たれている[1]。また、5月8日の5類移行に伴い、社会全体のアフターコロナに向けた動きが強まっている。一方、全国の陽性率は3月下旬から増加傾向にあり、地域によっては報告数が下げ止まりから増加傾向に転じている[2]。このような状況において、一部の専門家の間で再流行の可能性が指摘されている[3]。
COVID-19は、ワクチン接種および自然感染による集団免疫を維持することでコントロール可能である。本研究グループは、これまで数理モデルを用いて、国内のCOVID-19の集団免疫レベルの推計を継続的に行ってきた[4]。従来のモデルは、自然感染由来の免疫とワクチン由来の免疫の減衰の推移をそれぞれ把握できる点で現実的であったが、以下の2点に注意が必要であった[5]:
・自然感染とワクチン接種をいずれも経験した人の免疫(ハイブリッド免疫)の減衰は考慮していない。
・再感染は考慮していない。
これらの問題があるため、従来のモデルでは集団免疫レベルの過大評価に繋がる可能性があると考えられていた[5]。本稿では、これらの問題を改善した新たなモデルを構築し[6]、2023年5月1日現在の感染者報告数[1] およびワクチン接種数[7] のデータを用いて集団免疫レベルの推計を行う。また、その結果を2022年11月および2023年2月に厚生労働省(日本赤十字社が協力)によって実施された全国の抗体検査の結果[8] と比較する。
2.モデル
集団は、感染・ワクチンいずれも未経験(S)、感染のみ経験(I)、ワクチンのみ経験(V)、感染・ワクチンいずれも経験(W)の4種類に区分する。I、V、Wには通常の時間の他に滞在時間を導入し[9]、感染あるいはワクチン接種後の経過時間に応じて免疫が減少することを考慮している。また、免疫が減少することで再感染の可能性が高まるように設定している。更に、感染率も滞在時間に応じて変化するとしたうえで、潜伏期間および回復期間を決定している。
免疫の持続期間のデータは地域や株によってばらつきがあるが[10]、ここでは先行研究の結果 [10] [11]に従い、感染のみあるいはワクチンのみに由来する免疫の感染予防効果は半年で半減、感染とワクチンの両方に由来するハイブリッド免疫の感染予防効果は1年で半減すると仮定している。その他、モデルの詳細については付録[6]を参照されたい。
3.結果
モデルによる推計結果を図1に示す。
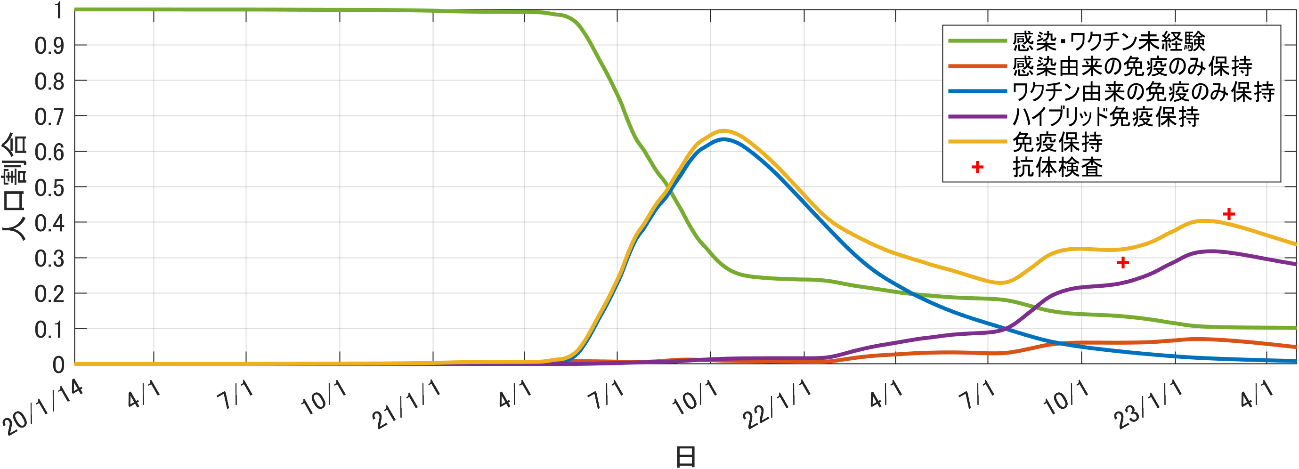
図1. COVID-19に対する国内の集団免疫レベルの推計結果
(2020年1月14日~2023年5月1日)
図1において、赤は感染のみに由来する免疫、青はワクチンのみに由来する免疫を保持する人口、紫は両者に由来するハイブリッド免疫を保持する人口の割合を表す。黄色はそれらの和であり、黄緑は感染・ワクチンいずれも未経験である人口の割合を表す。また、2022年11月および2023年2月にある赤の十字点は抗体検査の結果 [8] を表す。サンプリング・バイアスはあると考えられるが、すべての免疫保持者の割合を示す黄色の曲線は抗体検査の結果に近い値となっている。他方、第8波後の2023年2月以降は黄色の曲線が減少傾向にあり、第8波前の2022年10月の水準に近付いていることが読み取れる。よって、免疫レベルが減少したタイミングでの再流行は十分考えられる。
4.まとめ
本研究の推計では、2023年5月1日現在、COVID-19に対する国内の免疫レベルが減少傾向にあることが示された。免疫レベルが減少したタイミングや季節性により、感染者数の増加という意味での再流行が起こる可能性はある。しかし、先行研究の結果から、免疫による重症化予防効果は保たれていることが予想されるため[12][13]、行動制限の必要性は低いと考えられる。具体的な対策は、感染者数の動向ではなく、入院者数や重症者数などの医療の逼迫具合に応じて判断すべきである。
上記の通り、自然感染やハイブリッド免疫の重症化予防効果は長期に亘って持続するため、重症者や死亡者の数は第8波以上には増えないことが予想される。ただし、軽症であっても感染者数が増えれば高齢者などのハイリスク群の感染者が増え、結果として重症者数や死亡者数が増える可能性はある。特に、介護施設などの高齢者などにおいては、COVID-19肺炎による直接死亡ではなく、感染を契機に衰弱し、死に至るような間接死亡が多いと考えられる。5類への変更を契機に、拠点病院ではなく、地域において、こうした脆弱な層を守ることができる体制が必要である。
一方、ワクチン接種率が低く、自然感染例の少ない小児は、今後全体の感染者数を押し上げる可能性があり、小児の感染者数が増えて外来機能が逼迫すれば、医療に影響を与えるリスクがある。
今回の分析では、自然感染のみ、あるいは、ワクチンのみに由来する免疫は半年で、両者に由来するハイブリッド免疫は1年で感染予防効果が半減すると仮定した。一般に、ワクチンよりも自然感染の方が、持続効果の高い細胞性免疫を獲得しやすい傾向があると言われている[14] 。そのため、各免疫よりもハイブリッド免疫の持続期間の方が長いという仮定自体は妥当であると考えられる。ただし、この仮定が変われば、結果も変わる可能性があることに注意が必要である。
本研究では、先行研究 [4] で考えられていなかったハイブリッド免疫の減衰および再感染を考慮し、モデルを修正した上で推計を行った。そのため、従来のモデルによる免疫レベルの過大評価という問題は改善されたと考えられる。一方で、ウイルス変異、行動制限、季節性などの影響は、依然考慮していない。これらの要因は過去のデータに基づく推計よりも、将来の予測を行う際に問題になる可能性がある。
今回の推計は日本全体を対象に行ったが、今後、都道府県等、より詳細な区分での状況を早期に把握し、迅速に対応するためには、5類移行後も、地域のいくつかの医療機関において、少なくとも週単位で必要なデータが収集されることが望ましい。そのためには、収集データを検査陽性率、重症化率、致死率等に限定し、医療機関に負荷のかからない方法を採用する等、サーベイランスの効率性を考えることが肝要である。また、ウイルスの変異を検出するための病原体サーベイランスを強化することも等しく重要だと考える。
参考文献
[1] WHO, Coronavirus (COVID-19) Dashborad, https://covid19.who.int/. 2023年5月7日閲覧
[2] moderna, 新型コロナ・季節性インフルエンザ リアルタイム流行・疫学情報, https://moderna-epi-report.jp/. 2023年4月26日閲覧
[3] NHK特設サイト, “第8波超の「第9波」の可能性も” 新型コロナ専門家会合有志, https://www3.nhk.or.jp/news/special/coronavirus/advisory-board/detail/detail_111.html. 2023年4月26日閲覧
[4] 國谷紀良, 徳田安春, 中村治代, 諸見里拓宏, 渋谷健司, 国内におけるCOVID-19の第8波ピーク後の集団免疫レベルの推計, https://www.tkfd.or.jp/research/detail.php?id=4184. 2023年4月26日閲覧
[5] 國谷紀良, 徳田安春, 中村治代, 諸見里拓宏, 渋谷健司, COVID-19の集団免疫レベルの低下と再流行時期の予測, https://www.tkfd.or.jp/research/detail.php?id=4094. 2023年4月26日閲覧
[6] 付録, https://www2.kobe-u.ac.jp/~tkuniya/appendix_230501. 2023年5月7日閲覧
[7] デジタル庁, ワクチン接種記録システム(VRS), https://info.vrs.digital.go.jp/. 2023年5月7日閲覧
[8] 厚生労働省, 第2回献血時の検査用検体の残余血液を用いた新型コロナウイルスの抗体保有率実態調査, https://www.mhlw.go.jp/content/10906000/001070846.pdf. 2023年5月1日閲覧
[9] 稲葉寿編, 感染症の数理モデル 増補版, 培風館, 2020
[10] COVID-19 Forecasting Team, Past SARS-CoV-2 infection protection against re-infection: a systematic review and meta-analysis, Lancet 401 (2023) 833-842. https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(22)02465-5/fulltext. 2023年5月8日閲覧
[11] J. Malato, Stability of hybrid versus vaccine immunity against BA.5 infection over 8 months, The Lancet Infectious Diseases 23 (2023) 148-150. https://www.thelancet.com/journals/laninf/article/PIIS1473-3099(22)00833-7/fulltext. 2023年5月8日閲覧
[12] De La Vega M, Polychronopoulou E, XIII A, Ding Z, Chen T, Liu Q, Lan J, Nepveu-Traversy M, Fausther-Bovendo H, Zaidan MF, Wong G, Sharma G, Kobinger GP. SARS-CoV-2 infection-induced immunity reduces rates of reinfection and hospitalization caused by the Delta or Omicron variants. Emerging Microbes & Infections 12 (2023) e2169198. https://doi.org/10.1080/22221751.2023.2169198. 2023年5月8日閲覧
[13] Bobrovitz N, Ware H, Ma X, Li Z, Hosseini R, Cao C, Selemon A, Whelan M, Premji Z, Issa H, Cheng B, Raddad LJA, Buckeridge DL, Van Kerkhove MD, Piechotta V, Higdon MM, Wilder-Smith A, Bergeri I, Feikin DR, Arora RK, Patel MK, Subissi L. Protective effectiveness of previous SARS-CoV-2 infection and hybrid immunity against the omicron variant and severe disease: a systematic review and meta-regression. Lancet Infectious Diseases 23 (2023) 556-567. https://doi.org/10.1016/S1473-3099(22)00801-5. 2023年5月8日閲覧
[14] Radbruch A, Chang H. A long-term perspective on immunity to COVID. Nature 595 (2021) 359-360. https://www.nature.com/articles/d41586-021-01557-z. 2023年5月8日閲覧